メニュー
JP | JPY
-
-
-
- Challenges and Chances: A Review of the 1st Stem Cell Community Day
- Summertime, and the Livin’ Is Easy…
- Follow-on-Biologics – More than Simple Generics
- Bacteria Versus Body Cells: A 1:1 Tie
- Behind the Crime Scene: How Biological Traces Can Help to Convict Offenders
- Every 3 Seconds Someone in the World Is Affected by Alzheimer's
- HIV – It’s Still Not Under Control…
- How Many Will Be Convicted This Time?
- Malaria – the Battle is Not Lost
- Physicians on Standby: The Annual Flu Season Can Be Serious
- At the Forefront in Fighting Cancer
- Molecular Motors: Think Small and yet Smaller Again…
- Liquid Biopsy: Novel Methods May Ease Cancer Detection and Therapy
- They Are Invisible, Sneaky and Disgusting – But Today It’s Their Special Day!
- How Many Cells Are in Your Body? Probably More Than You Think!
- What You Need to Know about Antibiotic Resistance – Findings, Facts and Good Intentions
- Why Do Old Men Have Big Ears?
- The Condemned Live Longer: A Potential Paradigm Shift in Genetics
- From Research to Commerce
- Chronobiology – How the Cold Seasons Influence Our Biorhythms
- Taskforce Microbots: Targeted Treatment from Inside the Body
- Eyes on Cancer Therapy
-
-
-
-
- Challenges and Chances: A Review of the 1st Stem Cell Community Day
- Summertime, and the Livin’ Is Easy…
- Follow-on-Biologics – More than Simple Generics
- Bacteria Versus Body Cells: A 1:1 Tie
- Behind the Crime Scene: How Biological Traces Can Help to Convict Offenders
- Every 3 Seconds Someone in the World Is Affected by Alzheimer's
- HIV – It’s Still Not Under Control…
- How Many Will Be Convicted This Time?
- Malaria – the Battle is Not Lost
- Physicians on Standby: The Annual Flu Season Can Be Serious
- At the Forefront in Fighting Cancer
- Molecular Motors: Think Small and yet Smaller Again…
- Liquid Biopsy: Novel Methods May Ease Cancer Detection and Therapy
- They Are Invisible, Sneaky and Disgusting – But Today It’s Their Special Day!
- How Many Cells Are in Your Body? Probably More Than You Think!
- What You Need to Know about Antibiotic Resistance – Findings, Facts and Good Intentions
- Why Do Old Men Have Big Ears?
- The Condemned Live Longer: A Potential Paradigm Shift in Genetics
- From Research to Commerce
- Chronobiology – How the Cold Seasons Influence Our Biorhythms
- Taskforce Microbots: Targeted Treatment from Inside the Body
- Eyes on Cancer Therapy
-
JP | JPY
Sorry, we couldn't find anything on our website containing your search term.

細胞播種プロトコル – 細胞を正しく播種する方法のガイド
Lab Academy
- 細胞生物学
- 細胞培養
- 実験室の日常業務
- ピペッティングと分注
- 再現性
- ピペット
- チップ
- エッセー
細胞播種は通常、細胞ベースの実験においてプロトコルの最初のステップであり、標準手順です。 正確な標準化された細胞播種プロトコルは、再現性のある実験結果を得るのに重大な要素です。 このステップにおける主な課題は、繰り返し実験を行う際に、毎回同等の細胞数を達成し維持することです。
本記事は当初、細胞培養専門家向け月刊ニュースレター 『Inside Cell Culture』 に掲載されたものです。 他にも Co2 インキュベーターに関する興味深い記事があります。当サイトの 「CO2 インキュベーターに関する FAQ と資料」 ページでご覧ください。
Jessica Wagener 博士、Eppendorf細胞ハンドリングアプリケーションスペシャリスト
細胞播種は通常、細胞ベースの実験においてプロトコルの最初のステップであり、標準手順です。 正確な標準化された細胞播種プロトコルは、再現性のある実験結果を得るのに重大な要素です。 このステップにおける主な課題は、繰り返し実験を行う際に、毎回同等の細胞数を達成し維持することです。 細胞播種時の細胞数の変動や気泡の発生は、標準偏差を増加させ、結果の信頼性が低下します。 このため、実験室で確固たる細胞播種プロトコルを確立する際には、いくつかの要素を考慮する必要があります。
例えば、細胞を15 mL試験管からマルチウェルプレートに播種するとき、全てのウェルに注入するのには時間がかかります。 細胞播種プロトコルでは、シングルチャンネルピペットを使用するかマルチチャンネルピペットを使用するかに関わらず、このプロセスが長引くほど、チューブ内で沈降する細胞が増加します。 したがって、チューブやリザーバー内の細胞懸濁液を攪拌しないで使用すると、ウェルごとに細胞数が変動します(図1)。
Jessica Wagener 博士、Eppendorf細胞ハンドリングアプリケーションスペシャリスト
目次
- 標準化された細胞播種プロトコルの影響
- 時間的要素と細胞沈降
- 動画: 正しいピペッティング技術
- 気泡の発生
- 動画: 細胞播種における気泡の形成を回避する方法
- 均質な細胞接着
- 細胞密度依存の挙動
なぜ細胞播種はあらゆる細胞培養実験において重大なステップなのか?
細胞播種は通常、細胞ベースの実験においてプロトコルの最初のステップであり、標準手順です。 正確な標準化された細胞播種プロトコルは、再現性のある実験結果を得るのに重大な要素です。 このステップにおける主な課題は、繰り返し実験を行う際に、毎回同等の細胞数を達成し維持することです。 細胞播種時の細胞数の変動や気泡の発生は、標準偏差を増加させ、結果の信頼性が低下します。 このため、実験室で確固たる細胞播種プロトコルを確立する際には、いくつかの要素を考慮する必要があります。
細胞播種プロトコルにおける時間的要素
例えば、細胞を15 mL試験管からマルチウェルプレートに播種するとき、全てのウェルに注入するのには時間がかかります。 細胞播種プロトコルでは、シングルチャンネルピペットを使用するかマルチチャンネルピペットを使用するかに関わらず、このプロセスが長引くほど、チューブ内で沈降する細胞が増加します。 したがって、チューブやリザーバー内の細胞懸濁液を攪拌しないで使用すると、ウェルごとに細胞数が変動します(図1)。 もっと読む
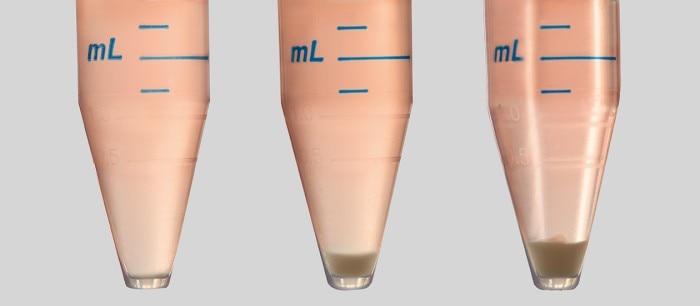
図1: 細胞沈降は、あらゆる細胞播種プロトコルにおいて考慮すべき重大な要素です。 容器内の細胞は数分以内に沈降します。細胞播種プロセスが長引くほど、上清中の細胞数は減少します。
細胞の沈降プロセスは非常に速く、数分以内に起こります。 この影響を避けるため、細胞を播種する前によく混ざるよう再懸濁または攪拌し、均質な溶液を調製する必要があります。 この方法で、ウェルごとの細胞数が確実に均等になります。
動画: 細胞播種プロトコルにおける正しいピペッティング技術
もっと読む
Videos not loading, because cookies have been rejected. Change your

細胞播種時の気泡の発生
細胞培養培地は、添加された血清のタンパク質含有量が高いため泡立ちやすくなっています。 気泡は細胞播種時の付着を妨げるため、ウェルごとの細胞数にばらつきが生じます(図2)。 特に96ウェルプレートや384ウェルプレートのような小型のプレートでは、ウェルあたりの培養面積が小さいため、気泡が大きな影響を与える可能性があります。 このため、再懸濁や攪拌は必須ですが過度に行ってはならず、ピペッティングもやりすぎないようにして気泡の発生を減らす必要があります。 穏やかにピペッティングすると、細胞にかかるせん断力とストレスを軽減できます。これはあらゆる細胞播種プロトコルにおいて重大な要素です。もっと読む
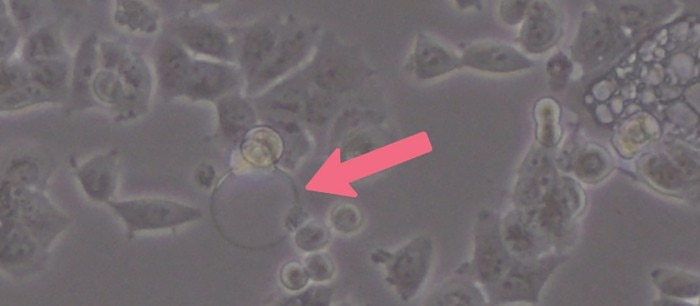
図2: 細胞播種時に発生する気泡は、細胞付着を妨げる可能性があります。 気泡の近くにある細胞が容器の底に適切に付着できないことに注目してください。
動画: 細胞播種における気泡の形成を回避する方法
もっと読む
Videos not loading, because cookies have been rejected. Change your

均質な細胞接着
均等な細胞数に加えて、培養容器の培養表面における均一な細胞分布も、実験結果に影響を与える可能性があります。 一般的な手法はさまざまで、通常は研究室で経験豊富な科学者から研修生へと受け継がれます。 しかし、細胞を培養表面に均一に分散させる最良の方法は何でしょうか? 図3で、異なる技法の比較をご覧ください。左側では、培養容器に細胞培養培地を充填してから、細胞を加えてそのまま放置した場合に何が起こるかがわかります。 結果として、細胞は主に容器の中央部に付着しています。 細胞分布を均等にするため、「8の字」の動きを用いる人もいれば、プレートやディッシュを十字状に動かす人もいます。 どちらの手法でも細胞の分布は改善されます。 しかし、容器の直径が小さくなるほど液体の動きは少なくなり、結果として細胞の分布が不均一になります。 細胞播種時にこの影響を回避する効果的な方法は、まず試験管またはリザーバー内で細胞懸濁液を所定の濃度に希釈(マスターミックス)し、その後最終的な量を培養容器へワンステップでピペッティングすることです。
もっと読む
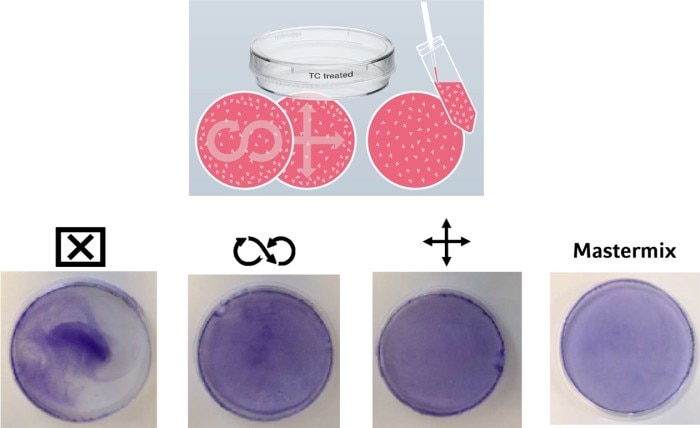
図3: さまざまな方法が存在し、その効率もさまざまで、いずれも培養容器に移し替えた後に細胞接着が確実に均一になるよう努めたものです。 最終細胞濃度のマスターミックスの使用が推奨されています。 細胞を固定し、クリスタルバイオレットで染色しています。
細胞密度は重要か?
細胞分布の均一性は、実験に重大な影響を及ぼすことがあります。 もちろん、均一な単層を形成するのではなく、コロニー状に増殖する傾向のあるタイプの細胞も存在します。 しかし、一般的には、細胞は培養容器の培養表面全体にできるだけ均一に広げるべきです。 細胞分布と細胞応答の直接的な影響を示す一例がトランスフェクション効率です(図4および図5)。もっと読む
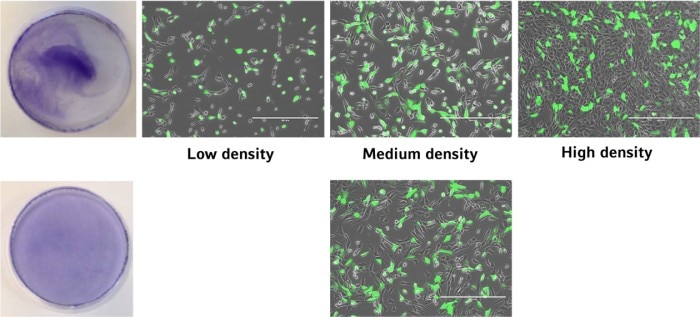
図4: 2種類の細胞播種法を用いた後の培養ディッシュ内におけるGFPトランスフェクション細胞の分布状況。
グラフに示すように、非トランスフェクト細胞に対するトランスフェクト細胞の比率が最も高くなるのは、細胞密度が中程度のときです。 さらに、マスターミックス法を用いた均一な細胞層の形成により、均一なトランスフェクション効率が得られます。 細胞播種プロトコルにおいて両方の要素を考慮することで、トランスフェクション効率を最適化し、標準偏差を低減できます。
もっと読む
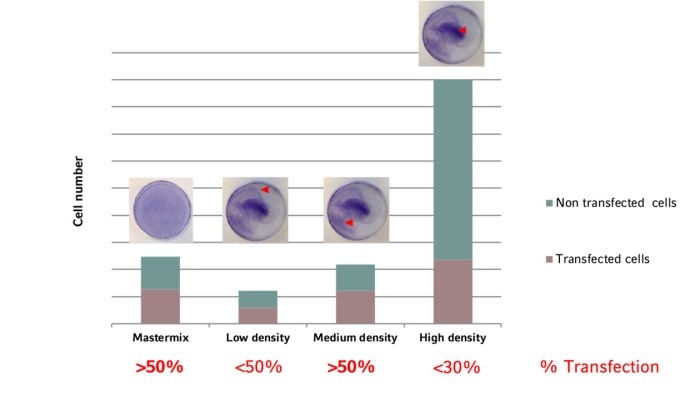
図5: トランスフェクション効率は細胞密度に依存します。 最適なトランスフェクション効率と均一な分布は、中程度の細胞密度とマスターミックス法との組み合わせによって達成されます。
